Fundamentación: asegurar
la calidad de los resultados de exámenes de laboratorio es un aspecto básico en
el derecho a la salud que el Estado debe garantizar.
Objetivo: determinar
la calidad de la toma de muestra de hisopado nasofaríngeo en pacientes críticos
con Covid-19 del área de laboratorio del Hospital IESS-Esmeraldas.
Métodos: se
realizó un estudio cuantitativo de corte transversal y alcance descriptivo,
entre octubre a diciembre de 2020. La población y muestra coincidieron y estuvo
comprendida por 42 usuarios (31 pacientes y 11 profesionales de la salud que
laboran en las instalaciones del laboratorio). Para la recolección de datos se
realizó una encuesta de satisfacción.
Resultados: El 36,36% de los laboratoristas indicaron que el
hospital cuenta con un sistema de calidad; sin embargo, el 27,27% de esta
población lo desconoce. Por otro lado, el 72,73% manifestó que en ciertas
ocasiones el hospital le brinda el equipo de protección personal. Asimismo, el
63,64% mencionó que a veces se le entrega insumos y reactivos. Con respecto al
usuario externo, el 51,61% indicó que nunca recibió recomendaciones después del
examen. El 29,09% coincidió en que el tiempo de espera para ser atendido es pésimo
y el 38,71% calificó la atención del laboratorio como regular.
Conclusiones: Se evidencia que no se cumplen con los
criterios de toma de muestra de hisopado nasofaríngeo
establecidos en los protocolos de calidad del
Hospital IESS-Esmeraldas.
Palabras
clave: muestras
nasofaríngeas; covid-19; pacientes críticos;
calidad; laboratorio.
Abstract
Background:
ensuring the quality of laboratory test results is a basic aspect of the right
to health that the State must guarantee.
Objective:
to determine the quality of nasal swab sampling quality in critical patients
with Covid-19 in the laboratory area of the
IESS-Esmeraldas Hospital.
Methods:
a descriptive cross-sectional quantitative study was carried out between
October and December 2020. The population and sample coincided and was
comprised of 42 users (31 patients and 11 health professionals who work in the
laboratory facilities). For data collection, a satisfaction survey was carried
out.
Results:
36.36% of the laboratories indicated that the hospital has a Quality System,
however, 27.27% of this population is unaware of it. On the other hand, 72.73%
stated that on certain occasions the hospital provides them with Personal
Protective Equipment. Likewise, 63.64% mentioned that supplies and reagents are
sometimes given to them. Regarding the external user, 51.61% indicated that
they never received recommendations after the examination. 29.09% agreed that
the waiting time to be seen is lousy and 38.71% described the laboratory care
as regular.
Conclusions:
It is evident that the criteria for taking the Nasopharyngeal Swab established
in the quality protocols of the IESS-Esmeraldas Hospital are not met.
Keywords:
nasopharyngeal samples; covid-19;
critical patients; quality; laboratory.
Calidad de la Toma de Muestra de Hisopado
Nasofaríngeo a Pacientes Críticos con Covid-19 en el Área de Laboratorio del Hospital
del IESS-Esmeraldas
De acuerdo con la Organización Mundial de la Salud [OMS] (2021), un sistema de
aseguramiento de la calidad implementado de manera adecuada permite asegurar
resultados confiables. Esto implica la creación y aplicación de lineamientos y
procedimientos estandarizados en toda la red de laboratorios que se deben efectuar
desde el instante en que se realiza la toma de muestra hasta cuando se tienen
los resultados para ser entregados a los pacientes. Esto se vuelve más
relevante en tiempos de pandemia como la que ocurre actualmente con la
aparición de la Covid-19, que ha puesto en riesgo la calidad de vida de la
población de manera universal.
La
sostenibilidad del sistema de gestión de calidad requiere de financiamiento
permanente, y de estrategias para mantener las actividades de aseguramiento de
la calidad, aun cuando disminuyera el número de casos de contagio por la pandemia
de la Covid-19.
La
predicción de la OMS (2013) fue evidente cuando en diciembre de 2019 se
reportaron los primeros casos de neumonía en Wuhan, China, causados por un
nuevo coronavirus, denominado como Covid-19. Este virus ha evolucionado
vertiginosamente hasta convertirse en una pandemia mundial, que ha demandado de
una acción inmediata en el desarrollo de las clásicas estrategias de salud
pública para enfermedades de orígenes virales, en especial, de afectaciones
respiratorias; y de la ejecución de un plan de atención médica en los distintos
niveles del Sistema Nacional de Salud.
La
Covid-19 es una enfermedad nueva dentro de las patologías existentes en el
sistema de salud. Estos coronavirus humanos (hCoV) son globalmente endémicos y
causan del 10 al 30% de las infecciones respiratorias agudas en adultos. Este
tipo de infecciones se consideraron generalmente leves hasta la aparición de
las epidemias del SARS (Síndrome Respiratorio Agudo y Grave) en 2002 y del MERS
(Síndrome Respiratorio del Medio Oriente) en 2012. Las dos provocaron índices
elevados de mortalidad en los países asiáticos. Por esta razón, en 2017, la OMS
(2013) los colocó en su lista de patógenos prioritarios.
Entonces,
es indispensable para los sistemas de salud contar con protocolos validados y
acordes con la realidad territorial y local que permitan al profesional poder
realizar la obtención de muestras Covid-19 de forma segura, cumpliendo con la
normativa de aseguramiento de la calidad para el análisis correspondiente,
evitando el contagio y propagación del virus. Esto indudablemente no existe en
el caso de estas enfermedades poco conocidas o cuyas manifestaciones clínicas
cambian a medida que se desarrollan.
La
obtención apropiada de las muestras es el primer requisito para generar un
análisis de calidad alta. No se puede obtener un buen resultado analítico
partiendo de una muestra deficiente. Asimismo, se hace necesario considerar
directrices establecidas en protocolos para la toma y remisión de las muestras,
siendo la tecnovigilancia la que garantiza la seguridad del paciente en todos
sus niveles para disminuir el riesgo de que los usuarios que acuden a sus
servicios sufran daños innecesarios durante la atención (Ortiz, Sánchez, &
Del Valle, 2010.
Los
servicios de salud son procesos complejos que incluyen a diferentes
profesionales, quienes utilizan variedad de tecnologías de acuerdo con la
necesidad de la morbilidad que atiendan, sin embargo, el riesgo de ocasionar
daño al paciente siempre está latente. Las tecnologías empleadas por los
profesionales de la salud dependen de la unidad de salud en la que están
desempeñando sus funciones, así como también del tipo de institución, sea esta
pública o privada. Todo este conjunto de herramientas se considera como
“dispositivos médicos” (OMS, 2009).
El
Ministerio de Salud Pública (MPS) estableció que el Instituto Nacional de
Investigación en Salud Pública (INSPI) cuenta con los reactivos necesarios para
la identificación de casos clínicos sospechosos, en asociación con el Centro de
Referencia Nacional de Influenza y otros Virus Respiratorios. El INSPI es una
organización acreditada por la OMS para la realización de pruebas que permitan
diagnosticar posibles casos de SARS-CoV-2, garantizando el Aseguramiento de la
Calidad entre los Servicios de Salud, Medicina Prepagada (ACESS) y la Agencia
Nacional de Regulación, Control y Vigilancia Sanitaria (ARCSA), efectuando
controles a los laboratorios que han sido autorizados para llevar a cabo las
pruebas de Covid-19 (Ministerio
de Salud Pública del Ecuador, 2020).
Según
la OMS (2013), toda prueba para detectar el Covid-19 debe efectuarse en
laboratorios que cuenten con los equipos adecuados y personal capacitado en
procedimientos técnicos y de seguridad pertinentes. Igualmente,
el personal encargado del transporte de las pruebas debe estar capacitado para
mantener la muestra en términos de tiempo y características hasta su entrega al
área de análisis. Todo el personal debe ser juicioso y responsable con sus funciones
para colaborar con los objetivos de calidad.
Cabe
destacar que teniendo en cuenta lo supra citado, para el área de laboratorio
del Hospital del IESS- Esmeraldas es prioridad el aseguramiento continuo de calidad
y calidez en sus servicios. Esta realidad se evidencia en los resultados
falsos positivos y negativos de Covid-19 que inciden en la calidad de vida de
la población, provocando altos índices de mortalidad.
De
acuerdo con la Sociedad
Española de Enfermedades Infecciosas y Microbiología Clínica [SEIMC]
(2020) los resultados pueden
ser falsos positivos, debido a la toma inadecuada de la muestra (frotis
nasofaríngeo), error preanalítico en el etiquetado de la muestra a lo largo del
proceso, retraso en el transporte, traslado inadecuado, contaminación cruzada
entre muestras durante el procesamiento. La compleja
problemática planteada tiene su origen en múltiples y diversas causas, entre
las principales están las siguientes:
ü La
ausencia de infraestructura;
ü La
falta de equipos por la dificultad para acceder a estos por sus costos
elevados;
ü Diferentes
marcas de productos, y;
ü Diversidad
de reactivos, lo que complica una adquisición segura y confiable.
Palacios
(2020) señala que una unidad de salud que no cuente con los suministros para la
toma de muestras y los medios adecuados para su traslado afecta el sistema de
diagnóstico. Por tanto, una toma inadecuada de la muestra en la que no se logre
acceder a la nasofaringe por no contar con varillas de algodón rígidas, el
resultado de la prueba será un falso negativo.
En
tal virtud, el Ministerio de Salud y
Protección Social de Colombia (2020)
señala que, las muestras deben ser tomadas por profesionales de la salud que
hayan recibido capacitación y entrenamiento en la toma de este tipo de muestras,
teniendo en cuenta todas las instrucciones de bioseguridad, incluido el uso de
los equipos de protección personal adecuados para virus respiratorios.
Se
hace ineludible admitir el compromiso de capacitación en la toma de muestra que
se tiene con el personal de los enfermeros, con el propósito de que estas
personas se encuentren técnicamente adiestradas para el debido procedimiento.
De igual manera, el no contar con protocolos estandarizados de procesos de
guías clínicas genera debilidad en el proceso de comunicación y monitoreo
continuo de la calidad institucional.
El
30 de enero de 2020, la OMS (2021) declaró al brote del nuevo coronavirus en la
República Popular China y los casos exportados a otros países como un Evento de
Salud Pública de Importancia Internacional (ESPII). Tiempo después, el 11 de
marzo de 2020 se declara a la Covid-19 como una pandemia mundial. Ante estos
anuncios, en Ecuador, mediante Acuerdo Ministerial Nro. 00126 –2020 se realiza
la declaratoria de estado de Emergencia Sanitaria en todo el territorio
nacional (9). Estas decisiones evidenciaron la magnitud del nuevo virus y la
necesidad de asegurar la calidad del tratamiento de las muestras de Covid-19 en
los laboratorios médicos de las instituciones de salud.
Gestión
de calidad
Los
criterios de calidad y de gestión han progresado significativamente en los últimos
setenta años. Juran (1990) destaca la importancia de la responsabilidad en la
administración con el propósito de perfeccionar el desempeño para satisfacer
las necesidades de los clientes. Entre las principales contribuciones, el autor
en mención, puntualizó la trilogía de la calidad que constituye un esquema de administración
funcional cruzado y que plantea tres procesos administrativos, estos son: organizar,
optimizar y conseguir niveles de prácticas cualificadas.
Por
su parte, Deming (1982) plantea los siguientes principios para garantizar la
calidad de una organización:
ü Crear
constancia de objetivos.
ü Adoptar
la nueva filosofía.
ü Eliminar
la dependencia de la inspección en masa.
ü Acabar
con la práctica de conceder un contrato sólo por su precio.
ü Mejorar
constantemente el sistema de producción y servicio.
ü Instituir
la formación y reformación.
ü Liderazgo.
ü Erradicar
el miedo.
ü Derribar
las barreras entre las áreas del personal.
ü Eliminar
lemas, exhortaciones y objetivos.
ü Eliminar
cuotas numéricas.
ü Eliminar
barreras para dignificar la fabricación.
ü Instituir
un programa de educación y reentrenamiento.
ü Actuar
para lograr la transformación.
En
la argumentación realizada por los autores antes citados, se aprecia que la
calidad es una propiedad que tiene múltiples significados y le confiere
capacidad a un objeto para satisfacer sus necesidades reales y sentidas. Para
James (1997) la gestión de la calidad es una filosofía de dirección generada
por una orientación práctica, que concibe un proceso que visiblemente ilustra
su compromiso de crecimiento y de estabilidad organizativa, es decir, una
acción que esté encaminada hacia el desarrollo de la calidad en el trabajo y a
la organización desde su totalidad.
Este
criterio de calidad es muy afinado, a pesar de los obstáculos asociados para el
cumplimiento de la misma. El aseguramiento de la calidad debe dotar al profesional
de técnicas y procedimientos que le otorguen la capacidad para orientar,
supervisar y controlar todas las etapas antes mencionadas hasta la obtención de
un producto de la calidad deseada.
Un
sistema de calidad debe enfocarse en asegurar que lo que promete una
organización es acorde con las especificaciones determinadas con anterioridad
por la empresa y el cliente, así se garantiza una calidad permanente en el
tiempo. Juran (1990) prepondera que la Norma ISO 8402 es el campo de
acciones planificadas y metodológicas que son imprescindibles para proveer
confianza de un producto o servicio que destaca por su calidad.
Riesgos
de calidad
La
Gestión de Riesgos tiene como prioridad detectar errores en los procesos antes
de que estos ocurran, aunque también permite proponer mejoras de desaciertos ya
ocurridos, de manera que se puede considerar una estrategia proactiva-reactiva
para la seguridad del paciente (13). Las técnicas de gestión de riesgos para
laboratorios clínicos se detallan y se integran como herramientas que permiten
identificar, prevenir y controlar errores que pueden causar daño al paciente
durante el proceso total de examen (Figueroa, 2015).
Notificación
de errores
La
notificación de eventos adversos en el laboratorio clínico se debe realizar a
través del sistema de gestión de calidad, aplicando verificaciones de rutina,
control de calidad, quejas y encuestas de satisfacción a usuarios. Estos
permitirán definir eventos, notificándose de manera oportuna a la casa de salud
y al proveedor de dispositivos médicos.
Mejora
de la calidad
La
articulación entre los proveedores y el laboratorio clínico debe
contribuir a mejorar la seguridad de los dispositivos médicos, incluyendo su
uso apropiado. El laboratorio debe priorizar las especificaciones esperadas de
un dispositivo médico de acuerdo con las necesidades de su proceso total de
examen. Estas se deben comunicar y socializar durante la selección y compra,
como parte los requisitos de la Institución de Salud para contribuir a la gestión
del sistema de calidad. Antes de usar los dispositivos con los pacientes o sus
muestras, estos deben ser verificados, bajo las condiciones ambientales y de
infraestructura requeridos, en función de las validaciones por el fabricante.
Una vez realizada la evaluación técnica de los dispositivos médicos, se
permitirá que la industria detecte oportunidades de mejora para sus procesos de
investigación y desarrollo, favoreciendo el resultado esperado por la casa de
salud en beneficio del usuario interno y externo.
El
aseguramiento de la calidad en los sistemas de salud
Según
Westgard y Migliarino (2014) la calidad de un laboratorio se mide realizando
control de calidad con eficacia y eficiencia. Para obtener resultados
analíticos de alta calidad, estos se encuentran obligados a estar garantizados
por el proceso de certificación a través de la Norma ISO 9001:2000. La
acreditación es un requisito que deben cumplir los laboratorios para demostrar
que poseen un sistema de calidad que garantiza la seguridad al usuario interno
y externo, por lo que hay que cumplir parámetros técnicamente competentes como
organización, control de la documentación, control de registros, control de
trabajos o calibraciones no conformes que sean capaces de generar resultados
técnicamente válidos.
El
ciclo que explica Deming adapta procesos como planear, hacer, verificar y
actuar. Este modelo es modificado por Burnett (2005) y comprende:
ü Organización
y gestión;
ü Gestión
de recursos:
ü Procesos
de exámenes de laboratorios;
ü Evaluación
y mejora.
Desde
estos principios, el laboratorio debe establecer y mantener procedimientos para
la identificación, recolección, codificación, acceso, archivo, almacenamiento,
conservación y eliminación de registros. Esto permitirá implementar políticas y
procedimientos cuando cualquier aspecto de su ensayo no cumpla con sus propios
procedimientos o con los requisitos acordados con el cliente. Díaz
(2020) afirma que la premura por pretender resolver las crisis solo potencia
las malas prácticas, pues ante la impotencia de perder la vida de los pacientes
se puede llegar a creer que cualquier medida, por más precaria que esta sea es
mejor a no tomar ninguna. Con esto sólo se justifica la atenuación de los
estándares de control y calidad que deben primar en la ciencia.
En
este orden de ideas, Drake (2020) expone que los métodos imperfectos y
materiales defectuosos han generado resultados poco confiables, así la primera
línea de diagnóstico para la enfermedad Covid-19 son los test genéticos de
anticuerpos. Precisamente, estos son los que han pasado por alto una proporción
considerable de los casos como consecuencia de los test imprecisos y no
autorizados que han inundado el mercado, debido a la ausencia de una
supervisión regulada.
La
calidad del análisis de muestras en el caso del Covid-19
La
Organización Panamericana de la Salud [OPS] (2020) en diciembre del 2019
comunicó que el SARS-CoV-2 es el agente etiológico responsable de un grupo de
casos de neumonía grave en Wuhan, China, identificado como un nuevo beta
coronavirus, distinto del SARS-CoV y MERS-CoV.
La
cadena genómica absoluta de este nuevo agente está disponible y se han acrecentado
distintos protocolos de identificación, a pesar de que no están autorizados por
completo. Sin embargo, a la luz de la circulación actual de Covid-19 en la
región de las Américas, la OPS y la OMS recomiendan a los Estados miembros
garantizar la detección apropiada de casos sospechosos, la obtención y la
remisión de muestras a los laboratorios, además de la incorporación de
protocolos de detección molecular, de acuerdo con el potencial del laboratorio.
El
19 de marzo de 2020, la OMS renovó la guía provisional sobre las pruebas de
laboratorio para la detección del Covid-19 en humanos con sospecha que incluye
información sobre la toma y envío de muestras, pruebas de laboratorio e
informes de casos y resultados. Igualmente, actualiza las definiciones de casos
sospechosos de Covid-19 según sea necesario.
La
OPS, en enero del 2020 informó que para cumplir con las medidas de bioseguridad
todo el personal del laboratorio debe usar equipo de protección personal (EPP)
apropiado que incluya mascarilla quirúrgica, guantes desechables, bata anti
fluidos y protección para los ojos que son necesarios para la manipulación de
muestras que son potencialmente infecciosas. Para la toma de una muestra
respiratoria de un paciente susceptible en Unidad de Cuidados Intensivos, se
debe utilizar la mascarilla N95. Los procedimientos de riesgo deben realizarse
en una cabina de seguridad biológica (BSC) de clase II. Deben usarse
dispositivos de contención física apropiados (por ejemplo: cubetas de seguridad
de centrífuga y rotores sellados) para la centrifugación. Notablemente, los rotores
para centrífuga deben cargarse y descargarse en el interior de una BSC.
El
profesional de la salud que desarrolla la gestión en Seguridad y Salud en el
Trabajo (SST), deberá recibir capacitación continua sobre las medidas de bioseguridad
y protección sobre la Covid-19, esta debe ser integral para todos los
trabajadores de una institución médica. La clasificación del nivel de riesgo
está elaborada en función de los puestos de trabajo existentes, sin embargo,
este nivel de riesgo puede variar dependiendo de las actividades que se le
asignen dentro del período de emergencia, por lo cual, el director podría
solicitar la modificación del nivel de riesgo de algún otro puesto de trabajo o
persona.
La
detección molecular de la Covid-19 aplicando protocolos correctamente delineados
suele ser bastante concreta; por ende, un resultado positivo corrobora la presencia
del virus. En contraste, un resultado negativo no siempre está vinculado a la inexistencia
de la infección por Covid-19. Varias razones pueden explicar un resultado
negativo en una persona infectada con el nuevo virus, principalmente:
ü Calidad
de la muestra;
ü Manipulación
y transporte, y;
ü Almacenamiento
deficiente.
Las
muestras deben arribar al laboratorio en la brevedad del caso, inmediatamente
después de haberlas tomado. Jamás se reclamará exageradamente en la importancia
de la administración adecuada durante la transportación. Cuando existe la
probabilidad de un retraso en la admisión de las muestras nasofaríngeas por el
laboratorio, se recomienda congelar las muestras y despacharlas en hielo seco.
No obstante, es muy importante tratar de no congelar y descongelar las muestras
varias veces. Debe evitarse el acopio de muestras de las vías respiratorias y
de suero en frigoríficos domésticos sin escarcha, debido a las elevadas oscilaciones
de temperatura.
El
Ministerio de Salud de Colombia (2020) advierte que los hisopos deben
disponerse y transportarse en un mismo tubo con medio de transporte viral.
Todas las muestras clínicas deben conservarse a temperatura de refrigeración,
es decir, entre -2 a 8°C, y después de las 48 horas deben permanecer congeladas
(temperatura de -70°C). El tiempo máximo de conserva de una muestra en
refrigeración es de 72 horas. Para el transporte de las muestras se debe
emplear geles o pilas congeladas. Se debe tener en cuenta que no conservar la
cadena de frío durante el transporte de la muestra, por ejemplo, con
temperaturas superiores a 8°C degrada la partícula viral, obteniéndose falsos
negativos.
Todos
los laboratorios nacionales de salud pública calificados para el diagnóstico
molecular, incluso los NIC, han implementado protocolos para la identificación
de la Covid-19. A tales efectos deben garantizar la disponibilidad de recursos
humanos e insumos genéricos (por ejemplo: kits de extracción y enzimas de
RT-PCR) para la detección del virus y planificar un aumento en las pruebas de
laboratorio.
Con
respecto a estudios previos, no se encontraron antecedentes en forma de
investigaciones directamente relacionadas con el tema tratado. A pesar de ello,
se asumieron como tales los siguientes: Ramírez y Herrera (2020) en su artículo
analizan el rol del laboratorio clínico ante la epidemia del Covid-19, en el
contexto de Costa Rica, con base a un estudio documental acerca de la técnica
en la toma de la muestra, el tipo de la muestra y otras variables preanalíticas;
así como las limitaciones intrínsecas del método en la interpretación de los
resultados, pues estas pruebas están sujetas a falsos negativos. Se pudo
revelar que se cuenta con poca diversidad de tecnologías para detectar la
Covid-19. Por este motivo es importante valorar la diversificación de las
pruebas de laboratorio y a la población a la que se aplicarán, pues Costa Rica
debe apoyarse en todas las herramientas diagnosticadas que permita el mercado,
teniendo en cuenta las limitaciones, especificidad, sensibilidad analítica y
clínica del método.
Por
su parte, Santo (2014) realizó una tesis doctoral acerca de la gestión de
calidad en el laboratorio clínico en 10 años de evolución, cuyos objetivos
fueron definir y desplegar diferentes indicadores en la perspectiva de proceso
interno del laboratorio para el servicio de análisis clínico del Hospital
Universitario de San Juan de Alicante; así como describir y analizar
retrospectivamente el comportamiento de los indicadores propuestos para las
distintas etapas del proceso analítico a lo largo de diez años.
El
estudio que se llevó a cabo fue de carácter observacional, descriptivo y
longitudinal, con base en las pruebas realizadas en el laboratorio de
bioquímica y hematología en dicho período; en nueve centros de salud de
atención primaria, un centro de especialidades y de pacientes de consultas
externas. Los registros y el cálculo de indicadores son recogidos y computarizados
automáticamente del SIL mediante una aplicación informática basada en
Datawarehouse y cubos OLAP (On-line Analytical).
Se
pudo concluir que los indicadores establecidos: preanalíticos de adecuación de
la demanda y de identificación del paciente; aceptabilidad de las muestras y
mensajerías; indicadores analíticos del proceso analítico en sí; indicadores
post- analíticos de medida del tiempo de respuesta e indicadores post- analíticos
de registro de resultados por aviso crítico son un instrumento útil para medir
la evolución de los procesos de laboratorio clínico y la identificación de
cualquier desperfecto u oportunidad de mejora.
El
problema actual es que el laboratorio clínico se ha industrializado de tal forma
que se crean millones de datos desamparados y susceptibles de malas
interpretaciones, capaces de esconder a aquellos que verdaderamente tienen relevancia
clínica. Por otro lado, es en la fase analítica donde se cometen menos errores,
pero es también donde se producen efectos más adversos. También se requiere
mejorar el tiempo de respuesta, especialmente en el laboratorio de urgencias.
Por
su parte, la OMS (2016) publicó un Manual acerca de un Sistema de Gestión de la
Calidad en el Laboratorio (LQMS) en el que se plantean las consecuencias
negativas de un error de laboratorio como son los tratamientos innecesarios,
complicaciones del tratamiento, tratamiento inadecuado, retraso en el
diagnóstico correcto y pruebas diagnósticas adicionales e innecesarias. En
consecuencia, se incrementan los gastos tanto en tiempo como esfuerzos del
personal, y a menudo dan lugar a malos resultados para el paciente.
Por
consiguiente, se plantea un modelo de Sistema de Gestión de Calidad definido
como las actividades coordinadas para dirigir y controlar una organización con
respecto a la calidad y en base a las normas ISO y Normas Clínicas de Laboratorio
(CLSI). Las actividades de laboratorio se establecen en 12 elementos claves:
organización, personal, equipos, compra e inventarios, gestión de procesos,
gestión de la información, documentos y registros, gestión de incidencias,
evaluación, mejora continua de procesos, servicios al cliente, seguridad e
instalaciones. Como se puede apreciar existen referencias suficientes con
relación a la importancia del aseguramiento de la calidad en los laboratorios
clínicos; y manuales o lineamientos para intentar asegurar la calidad en el
manejo de la Covid-19, pero no se halla una investigación específica como la
que se plantea.
Por
lo expuesto, el presente estudio favorecerá a la determinación de los factores
que incidieron en la calidad de la obtención de muestras de Hisopado Nasofaríngeo
tomadas en el laboratorio del Hospital del IESS-Esmeraldas. Además, se podrá
establecer la importancia de la preparación del personal profesional, y la
implementación de un protocolo, insumos, medidas de bioseguridad, al igual que
procesos y procedimientos para el tratamiento adecuado de las muestras. Es
preciso hacer énfasis que si no se cumple con estas condiciones se afectará
negativamente en la calidad de la muestra, y por ende los resultados que se
obtengan no serán de confianza.
Esta
investigación contribuirá al cumplimiento de la seguridad tanto en el personal
de salud como en los pacientes, siendo esta la prioridad en la obtención de la
muestra de hisopado nasofaríngeo en pacientes hospitalizados. De ahí que, la
novedad de este estudio radica en identificar si las técnicas aplicadas en
ausencia de un proceso seguro y ante una nueva enfermedad, han permitido
procesar muestras para la detección del Covid-19 sin riesgos de contagio a los
profesionales de la salud y a los usuarios que acuden al Hospital del
IESS-Esmeraldas. Cabe mencionar que si la aplicación de técnicas se realiza
cumpliendo con los protocolos de bioseguridad y los debidos procedimientos se
asegurará la calidad las muestras tomadas y se reducirá el riesgo de exposición
de contagio de quienes laboran y buscan atención médica en este hospital.
El
objetivo de este estudio es determinar la calidad de
la toma de muestra de Hisopado Nasofaríngeo en pacientes críticos con Covid-19
del área de laboratorio del Hospital IESS-Esmeraldas. Así, las
interrogantes que guiaron este proceso de investigación fueron:
ü ¿Cuál fue la calidad de la muestra
obtenida a través del Hisopado Nasofaríngeo aplicado por los profesionales de
la salud del área de laboratorio clínico del Hospital IESS-Esmeraldas?
ü ¿El personal de la salud del área de
laboratorio clínico del Hospital IESS-Esmeraldas fue capacitado para la toma de
muestras nasofaríngeas?
ü ¿Cuáles fueron las condiciones de insumos
y reactivos de laboratorio disponibles para la correcta toma de muestra de
Hisopado Nasofaríngeo?
ü ¿Cuáles fueron las causas por las que los
profesionales de la salud no utilizaron prendas de protección en el laboratorio
clínico de acuerdo con la norma técnica?
Método
Se
realizó un estudio cuantitativo de corte transversal y alcance descriptivo
entre octubre a diciembre del 2020. La población estuvo comprendida por 42
usuarios (31 pacientes y 11 profesionales de la salud que laboran en las
instalaciones del laboratorio).
Se
consideró como población a los pacientes en estado crítico que fueron atendidos
en el Hospital IESS-Esmeraldas y que se sometieron al procedimiento de hisopado
nasofaríngeo para la detección de Covid-19, así como el personal del
laboratorio del Hospital IESS-Esmeraldas que expresaron su consentimiento para
participar en la investigación.
Las guías de encuesta se elaboraron en Google Forms y a través de
un enlace fueron facilitadas a los pacientes y al personal de laboratorio.
 La encuesta de satisfacción del usuario externo fue tomada y
adaptada del modelo presentado por la Empresa
Social del Estado Hospital San Pedro y San Pablo La Virginia Risaralda,
aprobada en el 2009. El modelo de encuesta de satisfacción del usuario interno
corresponde al propuesto por Ávila y Malambo (2014).
La encuesta de satisfacción del usuario externo fue tomada y
adaptada del modelo presentado por la Empresa
Social del Estado Hospital San Pedro y San Pablo La Virginia Risaralda,
aprobada en el 2009. El modelo de encuesta de satisfacción del usuario interno
corresponde al propuesto por Ávila y Malambo (2014).
En
reunión con los directivos del Laboratorio Clínico del Hospital se explicó el
propósito y los fines de la investigación para certificar la ausencia de
conflicto de intereses. De igual forma, se aseguró que la información obtenida
será tratada con total responsabilidad y se utilizara exclusivamente con fines
de la investigación.
Resultados
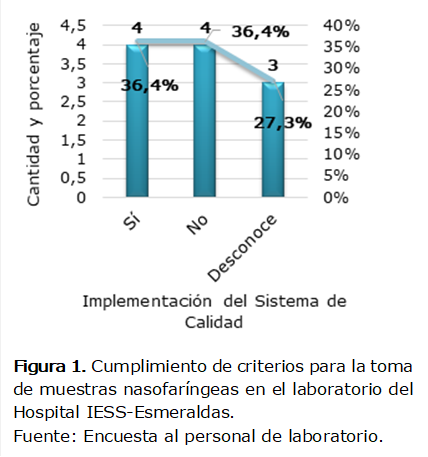
 Se
evidenció en la Figura 1 que el 36,4% (4 laboratoristas) indicó que sí se están
cumpliendo con los criterios para la toma de muestras nasofaríngeas, y también
el 36,4% respondieron que casi siempre, el 9,1% (1 laboratorista) nunca, el 9,1%
(1 laboratorista) casi nunca y el 9,1% (1 laboratorista) siempre.
Se
evidenció en la Figura 1 que el 36,4% (4 laboratoristas) indicó que sí se están
cumpliendo con los criterios para la toma de muestras nasofaríngeas, y también
el 36,4% respondieron que casi siempre, el 9,1% (1 laboratorista) nunca, el 9,1%
(1 laboratorista) casi nunca y el 9,1% (1 laboratorista) siempre.
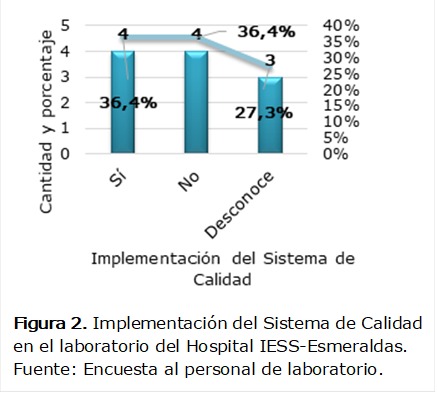
En
la Figura 2 se aprecia que el 36,4% (4 laboratoristas) afirmó que sí se ha
implementado en el hospital un Sistema de Calidad, el 36,4% (4 laboratoristas)
dijo que no y el 27,3% (3 laboratoristas) expresó que desconoce. De esto se
puede deducir que existen contradicciones en el personal sobre 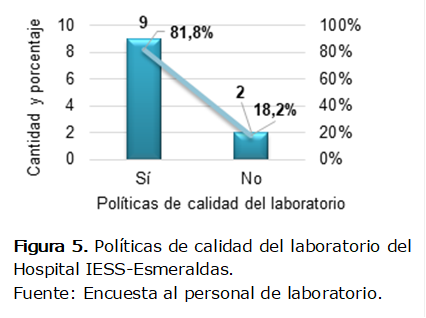 la
verdadera existencia de un Sistema de Calidad.
la
verdadera existencia de un Sistema de Calidad.
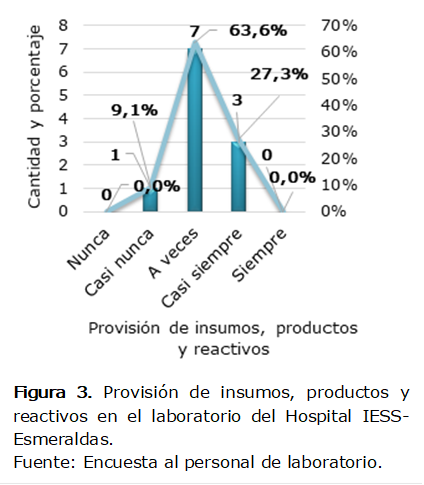
En
la Figura 3, el 63,6% (7 laboratoristas) manifestó que a veces el hospital le
brinda insumos, productos y reactivos con oportunidad y calidad para el desarrollo
de su trabajo. El 27,3% (3 laboratoristas) dijo que casi siempre y el 9,1% (1
laboratorista) expresó que casi nunca.
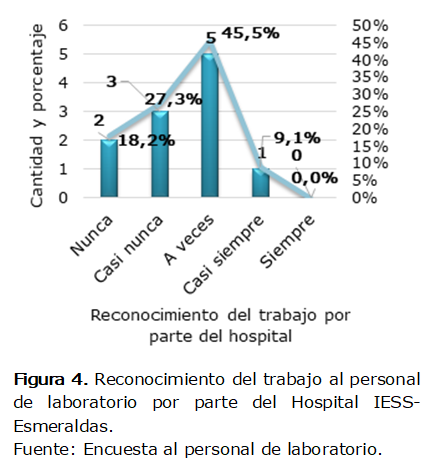 En
la Figura 4 se estima que el 45,5% (5 laboratoristas) a veces siente que su
trabajo es reconocido por el hospital, el 27,3% (3 laboratoristas) casi nunca,
el 18,2% (2 laboratoristas) nunca y el 9,1% (1 laboratorista) casi siempre.
En
la Figura 4 se estima que el 45,5% (5 laboratoristas) a veces siente que su
trabajo es reconocido por el hospital, el 27,3% (3 laboratoristas) casi nunca,
el 18,2% (2 laboratoristas) nunca y el 9,1% (1 laboratorista) casi siempre.
Asimismo,
en la Figura 5 se observa el conocimiento por parte del personal de laboratorio
acerca de las políticas de calidad de esta área. El 81,8% (9 laboratoristas)
manifestó que sí las conoce y el 18,2% (2 laboratoristas) expuso que no las
conoce. Esto revela que sí existen políticas en el laboratorio que son
mayormente conocidas por todo el personal.
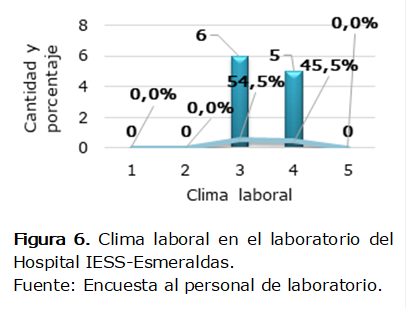 Con
respecto al clima laboral, en la Figura 6 se aprecia que el 54,5% (6
laboratoristas) lo califica de regular y el 45,5% (5 laboratoristas) indica que
es bueno.
Con
respecto al clima laboral, en la Figura 6 se aprecia que el 54,5% (6
laboratoristas) lo califica de regular y el 45,5% (5 laboratoristas) indica que
es bueno.
Entre
otras percepciones recolectadas por el personal de laboratorio se incluyen los
criterios que sugieren el mejoramiento de la infraestructura del área de toma
de muestra para hisopado nasofaríngeo, el aseguramiento de la calidad de la
muestra y la atención al paciente, debido a que se han generado muchos falsos
positivos y negativos, a lo que se suma el retraso en la entrega de resultados.
Los laboratoristas 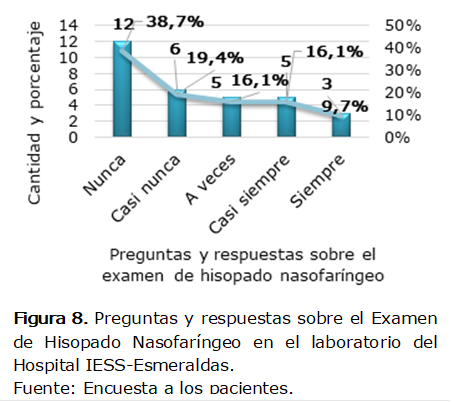 reconocieron
que al inicio hubo inconvenientes con el almacenamiento y transporte de las
muestras que en el transcurso se fueron corrigiendo, sin embargo, aún no logran
entregar resultados con prontitud. La falta de prendas de protección adecuadas
y la carencia de insumos siguen siendo un problema. Esta situación ha puesto en
riesgo la vida de los laboratoristas, pues todos se contagiaron de Covid-19, y
aunque superaron la enfermedad favorablemente, la exposición sigue siendo alta,
esto mientras no se garantice al personal un equipo de bioseguridad apropiado.
reconocieron
que al inicio hubo inconvenientes con el almacenamiento y transporte de las
muestras que en el transcurso se fueron corrigiendo, sin embargo, aún no logran
entregar resultados con prontitud. La falta de prendas de protección adecuadas
y la carencia de insumos siguen siendo un problema. Esta situación ha puesto en
riesgo la vida de los laboratoristas, pues todos se contagiaron de Covid-19, y
aunque superaron la enfermedad favorablemente, la exposición sigue siendo alta,
esto mientras no se garantice al personal un equipo de bioseguridad apropiado.
Los
resultados de la encuesta de satisfacción al usuario externo fueron los
siguientes:
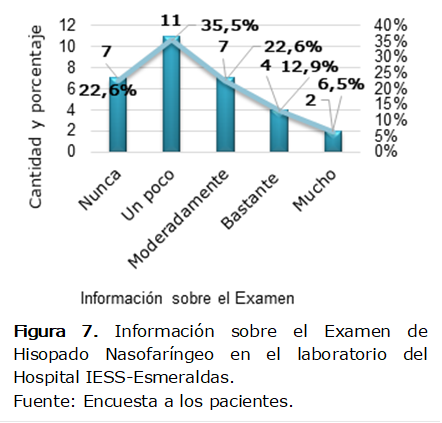 En
la Figura 7 se observa que el 35,5% (11 pacientes) declaró que la información
que recibió sobre el Examen de Hisopado Nasofaríngeo fue poca, el 22,6% (7
pacientes) indicó que nunca fue informado, el 22,6% (7 pacientes) dijo que
moderadamente. En su lugar, el 12,9% (4 pacientes) aseveró que se le brindó bastante
información y el 6,5% (2 pacientes) mucha.
En
la Figura 7 se observa que el 35,5% (11 pacientes) declaró que la información
que recibió sobre el Examen de Hisopado Nasofaríngeo fue poca, el 22,6% (7
pacientes) indicó que nunca fue informado, el 22,6% (7 pacientes) dijo que
moderadamente. En su lugar, el 12,9% (4 pacientes) aseveró que se le brindó bastante
información y el 6,5% (2 pacientes) mucha.
En
la Figura 8 se indica que el 38,7% (12 pacientes) confirmó que nunca el
personal de laboratorio les hizo preguntas sobre sus dudas ni tampoco se les
dio respuestas con conocimiento sobre el examen. El 19,4% (6 pacientes) expresó
que casi nunca, el 16,1% (5 pacientes) a veces, el 16,1% (5 pacientes) casi
siempre y el 9,7% (3 pacientes) siempre.
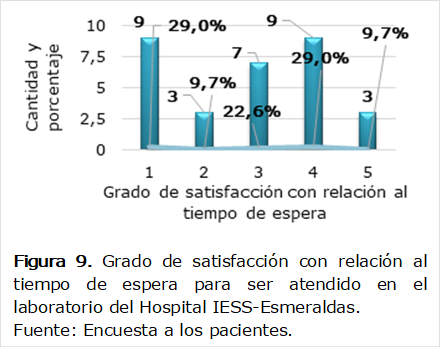 En
la Figura 9 se observa la calificación que los pacientes otorgaron con respecto
a su satisfacción por el tiempo de espera para ser atendidos. El 29% (9
pacientes) lo calificó de pésimo, el 29% (9 pacientes) de bueno, el 22,6% (7
pacientes) de regular, el 9,7% (3 pacientes) de malo y el 9,7% (3 pacientes) de
excelente.
En
la Figura 9 se observa la calificación que los pacientes otorgaron con respecto
a su satisfacción por el tiempo de espera para ser atendidos. El 29% (9
pacientes) lo calificó de pésimo, el 29% (9 pacientes) de bueno, el 22,6% (7
pacientes) de regular, el 9,7% (3 pacientes) de malo y el 9,7% (3 pacientes) de
excelente.
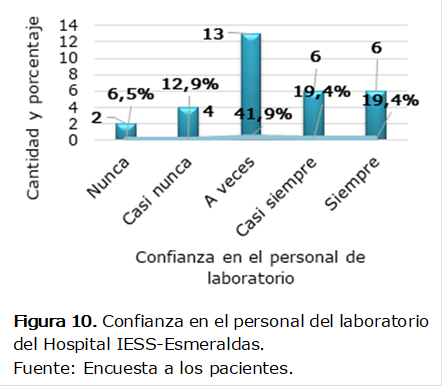 En
la Figura 10 se observa que el 41,9% (13 pacientes) considera que el personal
de laboratorio le inspira confianza a veces, el 19,4% (6 pacientes) casi
siempre, el 19,4% (6 pacientes) siempre, el 12,9% (4 pacientes) casi nunca y el
6,5% (2 pacientes) nunca.
En
la Figura 10 se observa que el 41,9% (13 pacientes) considera que el personal
de laboratorio le inspira confianza a veces, el 19,4% (6 pacientes) casi
siempre, el 19,4% (6 pacientes) siempre, el 12,9% (4 pacientes) casi nunca y el
6,5% (2 pacientes) nunca.
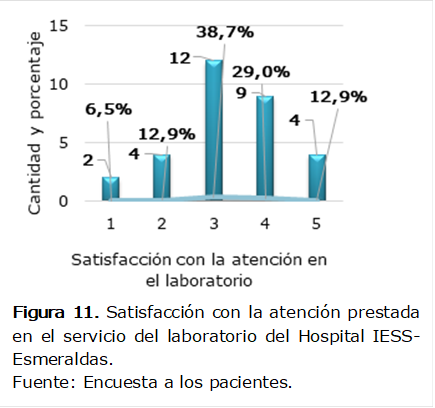
En
la Figura 11, el 38,7% (12 pacientes) calificó la atención prestada en el
laboratorio como regular, el 29% (9 pacientes) como buena, el 12,9% (4
pacientes) como mala, el 12,9% (4 pacientes) como excelente y el 6,5% (2
pacientes) como pésima.
Discusión
En
la investigación de Núñez (2020) titulada “Conocimiento y cumplimiento de las
medidas de bioseguridad del personal de la salud para la atención en paciente
Covid-19” se encontró que 8 de 20 artículos de Estados Unidos de América y 3 de
20 correspondientes a Irlanda tratan sobre el desabastecimiento del equipo de
protección personal y el incumplimiento de los protocolos para la colocación y
retiro de este equipo, situación que a nivel mundial está afectando al personal
de la salud que se encuentra en primera línea atendiendo los casos sospechosos
y confirmados de Covid-19. Estos resultados coinciden con los hallados en esta
investigación en la que se evidenció que el recurso humano del laboratorio del
Hospital IESS-Esmeraldas no dispone de prendas de protección adecuadas para
atender a los pacientes, y así evitar la propagación del virus entre los
usuarios internos y externos que participan de este servicio.
De
los 20 artículos que Núñez (2020) analizó, se encontró que solamente 8 daban a
conocer que la población que fue estudiada dispone de los conocimientos
pertinentes para tratar esta nueva enfermedad. Esto debido a que el personal
fue capacitado en medidas preventivas para la protección propia y la de los
compañeros de trabajo. En contraste, el personal sanitario que no fue capacitado
tuvo como consecuencia el contagio y el ausentismo laboral. Este evento fue
corroborado en la presente investigación, donde se determinó que un importante
porcentaje de los laboratoristas no fue capacitado, lo que trajo como
consecuencia que todos y todas se convirtieran en portadores del virus.
Núñez
(2020) resalta que debe existir una correlación entre los conocimientos del
personal de la salud con respecto al uso del equipo de protección personal y la
provisión del mismo, puesto que de nada sirve que se conozcan las medidas de
bioseguridad sino existen los recursos adecuados para su cumplimiento. Esta
situación también sería adversa si sucede lo contrario, es decir, si el
personal cuenta con los insumos y el equipo apropiado, pero desconoce su
correcta manipulación. Desde este análisis, en esta investigación se halló que
el personal de laboratorio del Hospital IESS Esmeraldas padece los dos
problemas, ya que no todos están aptos para brindar una atención segura y
tampoco cuentan con el equipo de protección suficiente.
Conclusiones
De
acuerdo con los objetivos y las preguntas de investigación planteadas se llegó
a las siguientes conclusiones:
Se
determinó que en el laboratorio del Hospital IESS-Esmeraldas existen
inconvenientes para el aseguramiento de la calidad en la toma de muestras de hisopado
nasofaríngeo que fueron aplicadas a pacientes críticos para el diagnóstico de
Covid-19 durante el periodo de octubre a diciembre de 2020.
Se
evidenció que no se cumple con los criterios y los estándares de calidad para
la toma y procesamiento de las muestras de hisopado nasofaríngeo que se
encuentran establecidos en los protocolos de calidad del Hospital
IESS-Esmeraldas. Esta situación generó falsos positivos y falsos negativos en
las pruebas.
El
personal del laboratorio del Hospital IESS-Esmeraldas no ha sido capacitado en
su totalidad para el diagnóstico de Covid-19, lo que ocasionó el uso inadecuado
de los recursos disponibles.
El
personal del laboratorio no dispuso de prendas de protección personal
suficientes, por lo que quedó expuesto a la infección del virus, derivando esto
en el ausentismo laboral.